质谱级赖氨酰肽链内切酶
Lysyl Endopeptidase®
本产品是质谱分析前处理时常用的蛋白分解酶即赖氨酰肽链内切酶,该酶可以特异性切除赖氨酸基团C末端的多肽,可用于蛋白测序分析和 Lys-X 化合物的酶合成。若同时使用赖氨酰肽链内切酶和胰酶,可更好地切断赖氨酸基团的多肽,增加多肽的数量。产品已按照使用习惯做成小包装,是方便使用的冷冻干燥品。20 μg/支可用于100-200个样品的凝胶内消化。
来源:细菌
外观:冻干粉(包含2 mmol/L Tris-HCl 缓冲液,pH8)
活性:0.03~0.07 AU/vial
分子量:27,000(琼脂糖过滤),30,000(SDS-PAGE)
溶解性:溶于水或缓冲液
稳定性:溶解于 pH 值 5.0-12.0 的 Tris 缓冲液中,可在4℃稳定保存2年;在 pH 值 6.0-11.0、30℃时能稳定保存,但温度超过50℃时不稳定。
最适pH值:9.0~9.5
等电点:6.9~7.0
底物特异性:
可水解底物——Tos-Lys-OMe、Bz-Lys-NH2、Bz-Lys-pNA、Lys-pNA
不可水解底物——Bz-Arg-NH2、Bz-Arg-pNA、Arg-pNA
抑制剂:DFP、PMSF、TLCK
◆特点
● 高特异性、高蛋白质消化率、适用于蛋白质谱分析
● 提高裂解效率、增加肽段数量
● 根据使用量特意制备小包装,方便使用
◆应用
分别采用胰蛋白酶(Tp)、赖氨酰肽链内切酶(Lys-C)和 Tp与Lys-C 联用进行胶内酶切的效果比较。
牛血清蛋白 BSA 的条带(100 ng)通过 SDS-PAGE 获得,然后分别用 Tp、Lys-C 和 Lys-C+Tp 进行酶切,再用 MALDI-TOFMS 法进行分析。
这些蛋白酶的实验效果见下表。
表 1:Tp、Lys-C 和 Lys-C+Tp 的结果对照
这些结果表明 Lys-C 酶解的漏切位点数(Missed Cleavage)最少。Tp 酶解时加入 Lys-C 后,漏切位点数有所降低,同时,可以鉴定出更多的多肽。
Tp | Lys-C | Lys-C+Tp | |
裂解位点 | 精氨酸和赖氨酸的C端 | 赖氨酸的C端 | 精氨酸和赖氨酸的C端 |
漏切位点数 (漏切位点所占比例) | 多(8%) | 很少(0%) | 少(3%) |
鉴定出的多肽数量 | 17 | 19 | 22 |
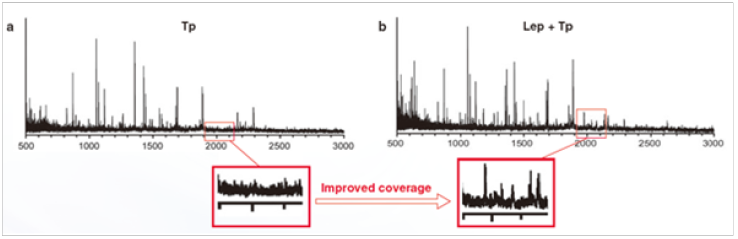
胰蛋白酶(Tp)(图 a)和赖氨酰肽链内切酶(Lys-C)+Tp( 图 b)酶切后的质谱结果对照图。
Lys-C+Tp 酶切后,可以在 m/z=2000 时得到吸收峰,而单独的 Tp 酶切在 m/z=2000 时没有吸收峰。该结果表明 Lys-C 可以提高测序覆盖度。
( 数据由大阪医疗中心和妇婴健康研究所Y. Wada 博士提供 )
赖氨酰肽链内切酶
赖氨酰肽链内切酶,最初由 Masaki 等人从土壤细菌中分离得到。该酶可以特异性剪切赖氨酸残基C末端和S-氨乙基半胱氨酸残基的肽键,用于蛋白测序和 Lys-X 化合物的酶催化合成。该酶稳定性高,在4M尿素或 0.1% SDS 溶液中 30℃ 孵育6小时之后,仍然拥有完整的生物活性。
外观 | 冻干粉(包含ca. 10% Tris-HCl buffer,pH 8) | 活性 | 见包装 |
分子量 | 27,000(凝胶过滤);30,000 (SDS-PAGE) | 溶解性 | 易溶于水或缓冲液 |
最佳pH | 9.0-9.5(酰胺酶的最佳活性 pH) | 等电点 | 6.9-7.0 |
抑制剂 | DFP、PMSF、TLCK | 来源 | 细菌 |
稳定性 | 溶于pH 值 5.0-12.0 的缓冲液中,可于4℃稳定保存。溶于pH 值 6.0-11.0 的缓冲液中,可于30℃稳 定保存,但是50℃及以上不稳定。 | ||
单位定义 | 一单位酰胺酶(AU)指在30℃ pH 9.5 时每分钟产生1 μmol 对硝基苯胺所需的酶量。 | ||
底物特异性 | 水解底物:Tos-Lys-Ome、Bz-Lys-NH2、Bz-Lys-pNA、Lys-pNA | ||
非水解底物:Bz-Arg-NH2、Bz-Arg-pNa、Arg-pNA | |||
※ 本页面产品仅供研究用,研究以外不可使用。
点此查看产品宣传页:质谱级赖氨酰肽链内切酶
实验方法
1. 试剂:
A.0.2 mol/L AMP 缓冲液,pH值 9.5
溶解 4.2 g 的2-氨基-2-甲基-1,3-丙二醇于 150 mL 的水中,加入1 mol/L HCl 调 pH 值至 9.5,再加水使体积至 200 mL。
B.2.5 mmol/L 底物溶液
溶解 22.6 mg 的α-Benzoyl-DL-lysine-p-nitroanilide Hydrobromide(产品编号:024-19731)于 20 mL 水中。
C. 2 mmol/L Tris-HCl 缓冲液,pH8
溶解 0.24 mg的2-氨基-2-羟甲基-1,3-丙二醇于 900 mL 水中,加入 0.1 mol/L HCl 调pH值至8,再加水使体积至1 L。
D. 酶溶液
溶解1vial 的赖氨酰肽链内切酶于1mL 的溶剂C中,可直接加入。
E. 终止溶液
将 55 mL 水和 45 mL 乙酸混合均匀。
2. 步骤
试剂 | 检测样品 | 空白对照 |
A | 2.6 mL | 2.6 mL |
B | 0.3 mL | 0.3 mL |
30℃ 预培养5分钟 | ||
D | 0.1 mL | - |
C | - | 0.1 mL |
立即混合均匀,30℃ 预培养25分钟 | ||
E | 1.0 mL | 1.0 mL |
3. 单位的定义
酰胺酶单位是指 30℃、pH 9.5 时,每分钟产生1μmol 对硝基苯胺的酶量。
AU/vial = [(a-b) / 25] × (1/9.62) × (4.0/0.1)
a. 检测样品中的吸光度
b. 空白对照中的吸光度
胶内酶切的实验操作流程
用聚硅酮处理的微量离心管和吸管端防止捕获任何蛋白。使用质谱分析用凝胶染色试剂盒,例如银染剂 MS 试剂盒(产品编号:299-58901)和负凝胶染色 MS 试剂盒(产品编号:293-57701)
1. 电泳分离蛋白质样品;
2. 从凝胶中切割蛋白质片断并放入微量离心管;
3. 使凝胶脱色(可使用质谱分析用凝胶染色试剂盒中的脱色溶液);
4. 加入300 μL 乙腈到试管里,搅拌器振荡 30 分钟;
5. 去除乙腈,用 Parafilm 膜覆盖微量离心管。
6. 在 Parafilm 膜上打出针孔,真空干燥 15 分钟;
7. 100 μL 10 mmol/L DTT 溶解于 100 mmol/L 碳酸氢铵,56℃恒温1小时。
8. 室温冷却后,用等量的 50 mM 碘乙酰胺溶解于 100 mmol/L 碳酸氢铵,暗处恒温 45 分钟并涡旋;
9. 用 100 μL 100 mmol/L 碳酸氢铵洗涤凝胶片段 10 分钟;
10. 用 300 μL 乙腈干燥凝胶片段 15 分钟;
11. 用 100 μL 100 mmol/L 碳酸氢铵溶胀凝胶片段 15 分钟;
12. 用 300 μL 乙腈再次干燥凝胶片段 15 分钟;
13. 去除液相,真空干燥凝胶片段 15 分钟;
14. 用 100 μL 赖氨酸内切酶溶液*在冰水浴中溶胀凝胶片段 45 分钟;
*赖氨酸内切酶稀释于 50 mmol/L Tris-HCl pH 8.5;
15. 去除 100 μL 赖氨酸内切酶溶液,将凝胶片段放在 37℃、10 μL 50 mmol/L Tris-HCl pH 8.5 中过夜;
16. 加入 50 μL 20mmol/L 碳酸氢铵 20 分钟内振荡凝胶片段3次抽提多肽;
17. 加入 5% 甲酸/50% 乙腈 20 分钟内振荡凝胶片段3次抽提多肽;
18. 如果需要用 Speed Vac. 浓缩多肽;
19. 用 ZipTip 脱盐和纯化多肽;
20. 如果需要用弱真空浓缩多肽至2 μL;
21. 加入基质进行质谱分析。
注意:根据细菌的生理和形态特征分类,产品来源为水解无色杆菌,但是最近细菌分类学将这种细菌鉴定为产酶溶杆菌。
保存:暗处-20℃保存
规格:20 μg×5 vial
相关产品
| 产品编号 | 产品名称 | 包装 | 应用 |
| 202-15951 | Trypsin, from Porcine Pancreas, Mass Spectrometry Grade 猪胰腺胰蛋白酶质谱级别 | 5×20 μg | 蛋白质组学 |
| 056-05921 | Endoproteinase Asp-N, Sequencing grade 胞内蛋白酶 Asp-N(测序级别) | 2 μg | 用于测序 |
| 050-05941 | Endoproteinase Glu-C, Sequencing grade 胞内蛋白酶 Glu-C(测序级别) | 50 μg | |
| 164-13982 | V8 Protease [Endoproteinase Glu-C] V8蛋白酶 | 2 mg | 生物化学 |

[1] Ojima T et al. “Characterization of Halomonas Sp. Strain H11 {alpha}-Glucosidase Activated by Monovalent Cations and Its Application for Efficient Synthesis of {alpha}-D-Glucosylglycerol.” Applied and Environmental Microbiology 78, no. 6 (March 15, 2012): 1836–1845.
[2] Leitner A et al. “Expanding the Chemical Cross-Linking Toolbox by the Use of Multiple Proteases and Enrichment by Size Exclusion Chromatography.”Molecular and Cellular Proteomics 11, no. 3 (March 1, 2012): M111.014126.
[3] Goetze A et al. “Rates and Impact of Human Antibody Glycation in Vivo.” Glycobiology 22, no. 2 (February 1, 2012): 221–234.
[4] Thingholm, T et al. “Characterization of Human Myotubes From Type 2 Diabetic and Nondiabetic Subjects Using Complementary Quantitative Mass Spectrometric Methods.” Molecular and Cellular Proteomics 10, no. 9 (September 1, 2011): M110.006650.
[5] Shoji M et al. “walK and clpP Mutations Confer Reduced Vancomycin Susceptibility in Staphylococcus Aureus.” Antimicrobial Agents and Chemotherapy 55, no. 8 (August 1, 2011): 3870–3881.
[6] Kubota T et al. “Quantitative Proteomic Analysis of Chromatin Reveals That Ctf18 Acts in the DNA Replication Checkpoint.”Molecular and Cellular Proteomics 10, no. 7 (July 1, 2011): M110.005561.
[7] Lee E et al. “The Steady-State Repertoire of Human SCF Ubiquitin Ligase Complexes Does Not Require Ongoing Nedd8 Conjugation.” Molecular and Cellular Proteomics 10, no. 5 (May 1, 2011): M110.006460.
[8] Shirai Y et al. “Direct Binding of RalA to PKC{eta} and Its Crucial Role in Morphological Change During Keratinocyte Differentiation.” Molecular Biology of the Cell 22, no. 8 (April 15, 2011): 1340–1352.
[9] Liu D et al. “N-terminal Glutamate to Pyroglutamate Conversion in Vivo for Human IgG2 Antibodies.” Journal of Biological Chemistry 286, no. 13 (April 1, 2011): 11211–11217.
[10] Shen H et al. “Constitutive Activated Cdc42-associated Kinase (Ack) Phosphorylation at Arrested Endocytic Clathrin-coated Pits of Cells That Lack Dynamin.” Molecular Biology of the Cell 22, no. 4 (February 15, 2011): 493–502.
[11] Keinath N et al. “PAMP (Pathogen-associated Molecular Pattern)-induced Changes in Plasma Membrane Compartmentalization Reveal Novel Components of Plant Immunity.” Journal of Biological Chemistry 285, no. 50 (December 10, 2010): 39140–39149.
[12] Maeda T et al. “Purification, Characterization and Amino Acid Sequence of a Novel Enzyme, D-threo-3-hydroxyaspartate Dehydratase, from Delftia Sp. HT23.” Journal of Biochemistry 148, no. 6 (December 1, 2010): 705–712.
[13] Rajagopal C et al. “Secretion Stimulates Intramembrane Proteolysis of a Secretory Granule Membrane Enzyme.” Journal of Biological Chemistry 285, no. 45 (November 5, 2010): 34632–34642.
[14] Sato H et al.“Novel Isonitrile Hydratase Involved in Isonitrile Metabolism.”Journal of Biological Chemistry 285, no. 45 (November 5, 2010): 34793–34802.
[15] Manno S et al. “ATP-dependent Mechanism Protects Spectrin Against Glycation in Human Erythrocytes.” Journal of Biological Chemistry 285, no. 44 (October 29, 2010): 33923–33929.
[16] Matsumoto T et al. “Proteomic Analysis Identifies Insulin-like Growth Factor-binding Protein-related Protein-1 as a Podocyte Product.” Renal Physiology 299, no. 4 (October 1, 2010): F776–784.
[17] Sury M et al. “The SILAC Fly Allows for Accurate Protein Quantification in Vivo.” Molecular and Cellular Proteomics 9, no. 10 (October 1, 2010): 2173–2183.
| 产品编号 | 产品名称 | 产品规格 | 产品等级 | 备注 |
| 125-05061 | Lysyl Endopeptidase®, MS Grade 赖氨酰肽链内切酶,MS级 |
20 μg×5 | 质谱级 | - |
| 121-05063 | Lysyl Endopeptidase®, MS Grade 赖氨酰肽链内切酶,MS级 |
20 μg | 质谱级 | - |
| 050-05941 | Endoproteinaseglu C, Sequencinggrade 测序级谷氨酰蛋白内切酶Glu-C |
50 μg | 生物化学分析级 | - |
| 202-15951 | Trypsin, from Porcine Pancreas, Mass Spectrometrygrade 猪胰腺胰蛋白酶质谱级别 |
20 μg×5 | 质谱级 | - |
| 免责声明 |
|
1. 本公司密切关注本网站发布的内容,但不保证发布内容的准确性、完整性、可靠性和最新性等。 2. 本公司不保证使用本网站期间不会出现故障或计算机病毒污染的风险。 3. 无论何种原因,使用本网站时给用户或第三方造成的任何不利或损害,本公司概不负责。此外,对于用户与其他用户或第三方之间因本网站发生的任何交易、通讯 3. 或纠纷,本公司概不负责。 4. 本网站可提供的所有产品和服务均不得用于人体或动物的临床诊断或治疗,仅可用于科研等非医疗目的。如任何用户将本网站提供的产品和服务用于临床诊断或治 4. 疗,以及其他特定的用途或行为,本公司概不保证其安全性和有效性,并且不负任何相关的法律责任。 |